Weiterführende Informationen und Differentialdiagnostik zur Zertifizierten Kasuistik "Patient mit unklaren Atembeschwerden"
von Herbert Jansen
Inhalt
Ergänzung zur Stufentherapie der Therapie des Asthma bronchiale
Diagnose
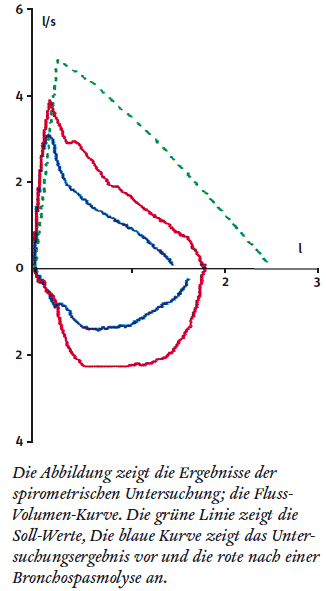
Bei der geschilderten Kasuistik handelt es sich um die Diagnose einer Erstmanifestation eines Asthma bronchiale im Kindes- und Jugendalter. Hierfür typisch sind das Auftreten nächtlicher Atembeschwerden mit Hustenattacken sowie auskultatorisch ein verlängertes Exspirium. Die dargestellte Fluß-Volumen-Kurve sichert die Diagnose. Der für eine obstruktive Ventilationsstörung typisch konkave Verlauf geht mit einer Erniedrigung folgender Parameter einher: PEF (Peak Flow), MEFx (Maximaler Fluss bei x% noch ausatembarer Vitalkapazität) und FEV1 (Einsekundenkapazität). Dabei ist in diesem Fall auch die Vitalkapazität konsekutiv als Zeichen einer mittelschweren Obstruktion erniedrigt. Zudem zeigt die durchgeführte Bronchospasmolyse mit Inhalation eines kurzwirksamen Beta-2-Sympathomimetikums (Salbutamol) eine partielle Reversibilität der Obstruktion.
Asthma bronchiale stellt die häufigste chronische Erkrankung im Kindesalter mit Prävalenzzahlen um 10 Prozent dar. Zu den Auslösern obstruktiver Symptome zählen im Kindesalter neben den inhalativen Allergenen vor allem
- virale Atemwegsinfektionen,
- körperliche Belastung,
- die Inhalation kalter trockener Luft und auch
- jegliche Form emotionalen Stresses.
Schon eine positive Familienanamnese für Atopie oder auch eine manifeste Atopische Dermatitis prädisponieren zu einer späteren Entwicklung eines Asthma bronchiale.
Differentialdiagnostik
Um andere Erkrankungen, die mit obstruktiver Symptomatik einhergehen, auszuschließen, ist im weiteren Verlauf der Diagnostik die Anfertigung eines Röntgen-Thorax notwendig. Hiermit sind beispielsweise kongenitale Anomalien oder andere chronisch entzündliche Veränderungen der Lungen zu diagnostizieren. Jedoch ist einschränkend zu erwähnen, dass Fehlbildungen der Bronchien oder der unteren Trachea in den meisten Fällen nur bronchoskopisch identifizierbar sind. Diese invasive Untersuchungsmethode steht allerdings am Schluss der diagnostischen Maßnahmen, falls trotz normaler bronchodilatatorischer Inhalationstherapie eine obstruktive Symptomatik persistiert.
Die Bestimmung des exhalierten Stickstoffmonoxids (FeNO) dient der Messung der (eosinophilen) Entzündungsreaktion in den Luftwegen. Beim unbehandelten beziehungsweise. nicht ausreichend antiinflammatorisch therapierten allergischen Asthma sind die FeNO-Werte entsprechend erhöht.
Neben der oben genannten Diagnostik sollte mittelfristig die Durchführung eines Schweißtests erfolgen, um eine Mukoviszidose auszuschließen. Da der Patient aber bislang keinerlei chronische pulmonale oder gastroenterologische Beschwerden hatte und normal (Größe und Gewicht jeweils im Normbereich) entwickelt ist, wäre die Diagnosestellung einer Cystischen Fibrose unwahrscheinlich.
In den dargestellten laborchemischen Befunden finden sich sowohl Zeichen einer allergischen Diathese mit erhöhtem Gesamt-IgE als auch einer spezifischen Sensibilisierung auf Birkenpollen und Katzenepithelien. Ob diese festgestellten Sensibilisierungen auch mit allergischen Symptomen einhergehen, bleibt abzuwarten beziehungsweise sollte mit Hilfe der Führung eines Symptometagebuchs einschließlich Peak-Flow-Protokolls weiter hinterfragt werden.
Anamnestisch sind jedenfalls rhinokonjunktivale Beschwerden im Frühjahr bekannt, die sicherlich durch die Sensibilisierung gegenüber Birkenpollen erklärbar sind. Diagnostisch weiterführend verbunden mit der Möglichkeit der Einleitung einer spezifischen Immuntherapie wäre hier die Durchführung einer nasalen Provokation mittels Rhinomanometrie.
Eine weitere seltene Erkrankung mit obstruktiver Symptomatik ist die Ziliendyskinesie. Diese Diagnose kann durch eine Funktionsuntersuchung der Zilien oder eine Elektronenmikroskopie einer Schleimhautbiopsie gesichert werden.
Zudem ist an die Möglichkeit eines nächtlichen gastro-ösophagealen Refluxes (GÖR) zu denken. Dieser stellt einen möglichen Triggerfaktor eines chronischen Asthma bronchiale dar und kann mittels einer kontinuierlichen pH-Metrie Messung über 24 h festgestellt werden.
Therapie
Nach entsprechender Aufklärung der Eltern des Patienten wurde eine inhalative Dauertherapie zunächst kombiniert mit einem Kortikosteroid und einem langwirksamen Beta-2-Sympathomimetikum (zum Beispiel Formoterol) in fixer Kombination eingeleitet. Nach drei Wochen zeigte sich in der durchgeführten Bodyplethysmographie eine weitgehende Normalisierung der obstruktiven Ventilationsstörung ohne Überblähungszeichen. Daraufhin erfolgte die Reduktion der Medikation im Sinne eines Step-down auf alleinige Dauertherapie mit einem inhalativen Kortikosteroid. Anamnestisch zeigte sich unter der beschriebenen Therapie eine gesteigerte allgemeine Leistungsfähigkeit ohne respiratorische Beschwerden auch bei körperlicher Anstrengung. Die symptomorientierte zusätzliche Applikation eines kurzwirksamen Beta-2-Sympathomimetikums (zum Beispiel Salbutamol, Reproterol, Fenoterol oder Terbutalin) beziehungsweise eines Anticholinergikums (zum Beispiel Ipratropiumbromid) konnte auf ein Minimum reduziert werden.
Begleitet wird die Dauertherapie vom regelmäßigen Führen eines Peak-Flow-Protokolls sowie eines Symptomtagebuchs insbesondere während der relevanten Pollenflugzeiten im Frühjahr. Langfristig wäre dann der Beginn einer Spezifischen Immuntherapie (SIT) zu erwägen. Die vorliegende Monosensibilisierung gegenüber Frühblüherpollen, die relativ kurze Erkrankungsdauer bzgl. der Pollenallergie und der offensichtliche Beginn einer Asthmaerkrankung sprechen für die Einleitung einer subkutanen SIT. Die Induktion neuer zusätzlicher Sensibilisierungen durch eine SIT ist nicht zu befürchten.
Ergänzung zur Stufentherapie der Therapie des Asthma bronchiale
In der aktuellen Fassung der fünf-stufigen Asthma-Therapie im Kindesalter wird die Medikamentengruppe der Cromone nicht mehr aufgeführt. Sie gelten als obsolet.
In der 2. Stufe werden entweder niedrig dosierte inhalative Corticosteroide (ICS) oder ein Leukotrienantagonist (LTRA, zum Beispiel Montelukast) eingesetzt.
Erst in Stufe 3 können LTRA als add-on zu ICS verwendet werden. Theophyllin stellt nur noch in Stufe 5 und auch dann nur in begründeten Ausnahmefällen eine therapeutische Option dar.
Ist in Stufe 3-5 eine Kombinationstherapie aus einem inhalativen Corticosteroid (ICS) und einem langwirksamen Beta-2-Sympathomimetikum (LABA) indiziert, werden im Kindes- und Jugendalter aus Compliance-Gründen, und um eine Monotherapie mit LABA aufgrund von Verwechslung oder Kortisonangst zu verhindern, zunehmend fixe Kombinationen bevorzugt. Hat sich unter inhalativer Dauertherapie zum Beispiel mit ICS in Stufe 2 eine Asthmaerkrankung stabilisiert, handelt es sich um ein kontrolliertes Asthma, so dass die Medikation in der Regel nach etwa drei Monaten reduziert werden kann.

