Weiterführende Informationen und Differentialdiagnostik zur Zertifizierten Kasuistik "Gangstörung, Immobilität im Alter und Sarkopenie"
von Michael Kowar, Kai Wilhelm und Andreas H. Jacobs
Inhaltsübersicht
Weitere Kasuistik zur Komplettierung des differentialdiagnostischen Spektrums
Weitere Kasuistik zur Komplettierung des differentialdiagnostischen Spektrums
Zur Komplettierung des Differenzialdiagnostischen Spektrums schildern wir noch einen zweiten Patienten, bevor es in die Erläuterungen geht.
Patient 2: Sturzneigung eines 87-jährigen Patienten mit Sarkopenie und kognitiven Einschränkungen. Anamnese: Die Einweisung des 87-jährigen Patienten erfolgte durch den Hausarzt aufgrund rezidivierender Stürze, Gewichtsverlust von circa 40 kg über zwei Jahre und fremdanamnestisch auffälligen Orientierungsstörungen. Körperliche Untersuchung: Patient mit fortgeschrittenen Zeichen der Sarkopenie und Exsikkose. Internistisch altersgerechte Organbefunde. Neurologisch diskretes beinbetontes Halbseitensyndrom rechts mit Betonung der Muskeleigenreflexe und Fußheberparese rechts. In den Zeige-, Stand- und Gangversuchen Zeichen der „higher level gait disorder“ mit ungerichteter Fallneigung ohne Hinweise auf sensible Ataxie. Psychisch ist der Patient nicht orientiert zur Zeit und wechselnd orientiert zur Situation mit Störungen von Auffassung und Gedächtnis. Neuropsychologische Testung: Minimental Status Test (MMSE) 17/28 Punkten, geriatrische Depressionsskala 2/15 Punkte. Labor: Routineparameter einschließlich Vitamin B12, Folsäure und Schilddrüsenfunktionswerte im Normbereich. CCT: Lakune im Thalamus links, Zeichen der SAE, kortikale Atrophie temporal beidseits (Abbildung 2). EEG: Zeichen der Allgemeinstörung. Duplexsonographie der Gehirnversorgenden Arterien: Zeichen der Arteriosklerose ohne Hinweis auf höhergradige Stenose. CT Thorax und Abdomen: Kein Hinweis auf Tumor. |
In den vorliegenden Fällen handelt es sich um den geriatrischen Problemkomplex der multifaktoriell bedingten, langsam progredienten Immobilität. Bei dem in der Kasuistik beschriebenen Patienten 1 liegt die Genese in einer Kombination aus einer lumbalen Spinalkanalstenose in Kombination mit schwerer Herzinsuffizienz, subkortikaler arteriosklerotischer Enzephalopathie (SAE) und Sarkopenie. Demgegenüber ist bei dem Patienten 2 die Genese in einer Kombination aus fortgeschrittener SAE und lakunärem Schlaganfall mit Sarkopenie zu sehen.
Einführung
Eine zunehmende Gangstörung mit rezidivierenden Stürzen und resultierender Immobilität ist ein typisches Syndrom beim geriatrischen, multimorbiden Patienten und gehört zu einem der zentralen „Is“ der Geriatrie (neben Instabilität, intellektuellem Abbau und Inkontinenz) (1). Die Gangstörung im Alter ist häufig nicht nur durch eine Ursache sondern meistens multifaktoriell bedingt. So spielen muskuloskelettale Veränderungen, Herz-Kreislauferkrankungen, neurologische und psychiatrische Erkrankungen eine große Rolle. Hinzu kommen im höheren Alter Sinnesstörungen im Rahmen von Presbyopie und Vestibulopathie. Im Rahmen ärztlicher Interventionen und von Medikamenten können Nebenwirkungen und Komplikationen auftreten, die das Gangbild weiter verschlechtern. Mögliche Ursachen von Gangstörungen im Alter sind in Tabelle 1 zusammengefasst.
| Tabelle 1: Ursachen für Gangstörungen | |
|---|---|
| Neurologische Erkrankungen | Hirninfarkt, „higher level gait disorder“ bei SAE, M. Parkinson, NPH, Multisystematrophie, Epilepsie, Polyneuropathie |
| Muskuloskelettale Veränderungen | Polyarthrose (speziell Cox-/Gonarthrose), Sarkopenie, Osteoporose, Frakturen, rheumatoide Arthritis, Polymyalgia rheumatica, zervikale oder lumbale Spinalkanalstenose |
| Sinnesstörungen | Katarakt, Glaukom, Maculadegeneration, Vestibulopathie, Presbyakusis |
| Herz-Kreislauferkrankungen | Herzinsuffizienz, KHK, Aortenklappenstenose, COPD, pAVK, Herzrhythmusstörungen |
| Iatrogen | Medikamente (v.a. mit sedierender Nebenwirkung), Hyponatriämie, Operationen |
| Psychiatrische Erkrankungen | Depression, Demenz, Sturzangst |
Die beschriebenen Störungen führen zu einer erhöhten Vulnerabilität und Verletzlichkeit, was zu der Gefahr des Verlustes der Selbständigkeit führen kann. Dies wurde bereits von Linda Fried in der Geriatrie unter dem Begriff Frailty (Gebrechlichkeit) beschrieben (2). Die Prävalenz von Frailty bei über 65 Jährigen liegt zwischen 6 und 27 Prozent, wobei Frauen fast doppelt so häufig betroffen sind wie Männer (3).
Wichtig als Ursache von Stürzen ist zusätzlich das Vorliegen einer Sarkopenie als altersassoziierter Muskelschwund (im Gegensatz zu Mangelernährung und Kachexie) und einem damit verbundenen Verlust von Muskelkraft (4). Diese kann nicht nur Ursache, sondern auch Folge einer Immobilität sein. Untersuchungen zeigen, dass 32 Prozent der Männer und 17 Prozent der Frauen über 65 Jahre von Sarkopenie betroffen sind (5).
Das Syndrom der drohenden Immobilität führt bei Fortschreiten neben Einschränkungen im physiologischen Bereich (Sarkopenie, Folgeerkrankungen, erhöhte Mortalität) auch zu Einschränkungen im sozialen Bereich (z. B. soziale Isolation). Häufig stehen im Zusammenhang mit Gangstörungen auch Einschränkungen von Stimmung und Kognition (6). Im Verlauf kommt es somit zu einem „circulus vitiosus“ der geriatrischen Is. Dieser ist mit einer verlängerten Krankenhausaufenthaltsdauer und erhöhten Mortalität assoziiert (7, 8).
Diagnostik
Wie bereits beschrieben, ist die Motorik und das Gehen durch einen komplexen Regelkreis (Netzwerk) des zentralen und peripheren Nervensystems gesteuert. Dabei finden sich neben den primären motorischen Impulsen über die Pyramidenbahn (betroffen nach Schlaganfall oder bei ALS) Schaltkreise über das Basalgangliensystem (betroffen bei z. B. M. Parkinson), das Kleinhirn (betroffen bei z. B. Multisystematrophie vom cerebellären Typ oder nach Schlaganfall) und spinale Systeme (betroffen bei z. B. Spinalkanalstenose). Rückkopplungen erfährt das motorische System über optische, vestibuläre und propriozeptive Afferenzen (betroffen z. B. bei Presbyopie, Vestibulopathie und PNP). Als supportive Strukturen leisten das Herz-Kreislauf-System und Muskeln, Bänder und Gelenke einen wesentlichen Beitrag zur adäquaten Ausführung einer motorischen Funktion (siehe Tabelle 1).
Um das führende Problem einer Gangstörung oder einer Gangverschlechterung zu verstehen und herauszufiltern, ist eine ausführliche klinische Anamnese und das geriatrische Assessment (GA) notwendig, um nicht nur unnötige Diagnostik zu vermeiden, sondern auch die geriatrische Therapie zu spezifizieren und zu personalisieren. Dabei kann das geriatrische Assessment als das „CT des Geriaters“ verstanden werden, mit dem dieser sich das bestmögliche Bild von der Problemstellung des Patienten machen will.
Beim Patienten 1 bestand seit längerem eine Immobilität, die zuletzt in einer Bettlägerigkeit endete. Da sich bereits Kontrakturen an den Füßen zeigten und die Beinbeweglichkeit eingeschränkt war, erfolgte zunächst eine radiologische Diagnostik der LWS. Hier zeigten sich fortgeschrittene degenerative Veränderungen mit Osteochondrose und lumbaler Spinalkanalstenose (siehe Abbildung 1B). Hinweise auf fortgeschrittene arthrotische Veränderung ergaben sich nicht.
Zum sicheren Ausschluss einer zentralen Gangstörung erfolgte ein MRT des Schädels. Hier zeigten sich vor allem vaskuläre Veränderungen im Sinne einer SAE (siehe Abbildung 1A). Hinweise auf einen Infarkt ergaben sich nicht. Dies war auch aufgrund der Anamnese eher unwahrscheinlich.
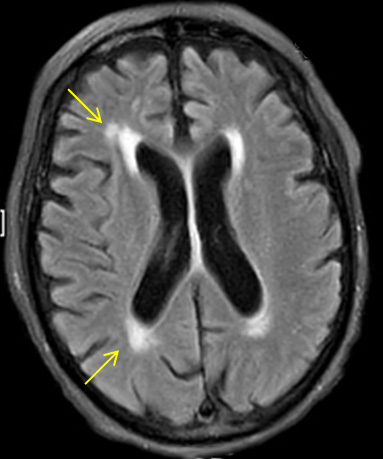
Abbildung 1A
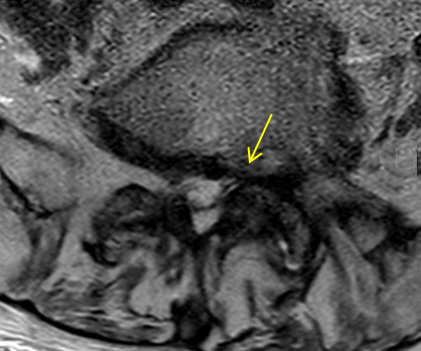
Abbildung 1B
Bildgebende Diagnostik des 74-jährigen Patienten mit multifaktoriell bedingter Immobilität. Im MRT Schädel (Abb. 1A) Zeichen der subkortikalen arteriosklerotischen Encephalopathie (SAE) als häufigste Ursache einer „higher level gait disorder“. Im MRT des Myelons (Abb. 1B) Zeichen einer fortgeschrittenen lumbalen Spinalkanalstenose mit linksbetonter Bandscheibendegeneration auf Höhe LWK 4/5. Quelle: Johanniter Krankenhaus Bonn.
Bereits in der radiologischen Untersuchung des Thorax bei Aufnahme zeigte sich ein global dilatiertes Herz. Zur weiteren Diagnostik erfolgte eine transthorakale Echokardiographie, in der sich eine bereits fortgeschrittene Kardiomyopathie mit reduzierter systolischer Pumpfunktion (EF 15%) zeigte. Dies zeigte sich auch klinisch im Rahmen von Beinödemen und einer reduzierten Belastbarkeit (Ruhedyspnoe).
Zusätzlich konnte bereits klinisch eine deutliche Muskelatrophie vor allem der Beine festgestellt werden, welche im Sinne einer fortgeschrittenen Sarkopenie zu werten ist.
Aufgrund der langsamen Progredienz der Beschwerden mit schließlich eingetretener kompletter Immobilität und Bettlägerigkeit lässt sich bei Patient 1 als primäre Ursache die lumbale SKS bei begleitender SAE, schwerer Herzinsuffizienz und Sarkopenie als multifaktorielle Ursachen für die Immobilität festhalten.
Beim Patienten 2 war es durch die bisher nicht wahrgenommene Fußheberschwäche rechts durch einen lakunären Infarkt im Bereich des hinteren Schenkels der Capsula interna links zu einem Sturz gekommen. Im Untersuchungsbefund dominierte darüber hinaus ein „wackeliges Gangbild“ als „higher level gait disorder“ durch SAE, die bildgebend verifiziert werden konnte (siehe Abbildung 2A). Komplettiert wurde das geriatrische Syndrom durch kognitive Einschränkungen am ehesten i.R. der temporal betonten Atrophie (siehe Abbildung 2B) basierend möglicherweise auf einer Alzheimererkrankung mit spätem Beginn.
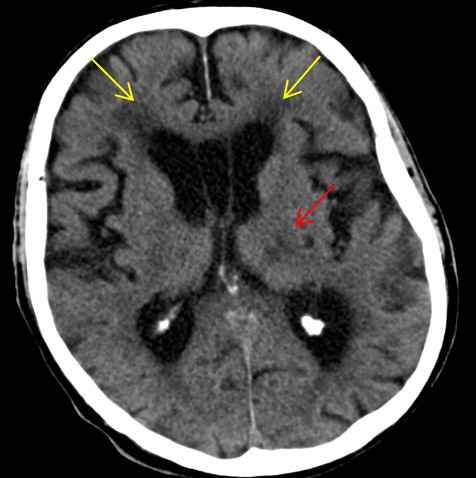
Abbildung 2A
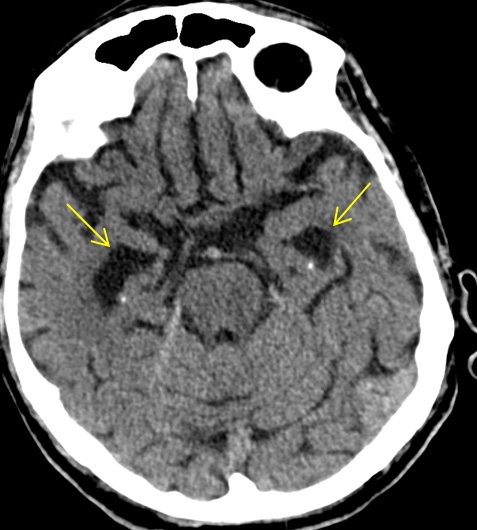
Abbildung 2B
Bildgebende Diagnostik des 87-jährigen Patienten mit multifaktoriell bedingter Gangstörung mit rezidivierenden Stürzen. Im CCT auf Höhe der Stammganglien (Abbildung 2A) Zeichen der subkortikalen arteriosklerotischen Encephalopathie (SAE) als häufigste Ursache einer „higher level gait disorder“ (gelbe Pfeile). Zusätzlich Zeichen eines lakunären Infarktes im hinteren Schenkel der Capsula interna links als Ursache für die Fußheberschwäche rechts (Auslöser für Sturz; roter Pfeil). Im CCT auf Höhe temporomesialer Strukturen (Abbildung 2B) Zeichen einer fortgeschrittenen temporal-betonten Atrophie als mögliche Hinweise für eine Alzheimer Demenz mit spätem Beginn (LOAD) als Ursache für die kognitiven Einschränkungen des Patienten.Quelle: Johanniter Krankenhaus Bonn
Therapie
Die geriatrische Therapie zielt immer auf eine Verbesserung der Funktion. Gemeint sind damit in der Regel Alltagsfunktionen (ADL). Damit sollen die Selbständigkeit gefördert und erhalten sowie die Pflegebedürftigkeit verhindert werden.
Der Patient 1 lehnte jegliche weitere kardiologische Diagnostik ab. Die Gefahr von malignen Herzrhythmusstörungen wurde genauso wie die Möglichkeit einer ICD-Implantation besprochen, aber vom Patienten nicht gewünscht. Dies unterstreicht die Notwendigkeit, in der funktionsorientierten geriatrischen Behandlung Wertvorstellungen von Patienten und Angehörigen in einer einvernehmlichen Behandlungsplanung zu berücksichtigen. Es erfolgte daher ein konservatives Procedere mittels Herzinsuffizienztherapie nach Leitlinie.
Beim Patienten 2 stand im Vordergrund die Behandlung der zerebrovaskulären Risikofaktoren in Kombination mit Gangtraining mit speziellem Fokus auf den rechten Fuß.
Zusätzlich erfolgte bei beiden Patienten eine medikamentöse Therapie der Sarkopenie mittels oraler Vitamin D3-Substitution. Die nicht-medikamentöse Therapie wurde in Form von Muskeltraining (Physiotherapie) und ADL-Training (Ergotherapie) durchgeführt. Hier wird als Ziel eine Kombination aus Ausdauer- (30 min/Tag) und Krafttraining (15 min jeden 2. Tag) zur Therapie der Sarkopenie empfohlen (9). Dabei ist auf eine ausreichende Proteinzufuhr (Milch- und Quarkprodukte) zu achten. Hierdurch soll die Funktionalität (ADL) verbessert werden, um damit weitere Stürze zu verhindern. Aufgrund der bereits bestehenden Bettlägerigkeit von Patient 1 beschränkte sich das Therapieziel auf die Verbesserung des Transfers. Im Bereich der Ergotherapie wurden Hilfsmitteltherapien im Rahmen der ADL durchgeführt. Aufgrund der Ulcerationen (Dekubiti III°) erfolgte eine entsprechende Wundversorgung.
Ergebnisse
Beim Patienten 1 konnte aufgrund der bereits fortgeschrittenen Immobilität (Bettlägerigkeit seit mehreren Wochen) mit einhergehenden Komplikationen (Ulcera, Kontrakturen) zumindest ein verlängertes Sitzen im Stuhl und ein erleichterter Transfer in den Stuhl (zuletzt mit einer Hilfsperson) erzielt werden. Damit wurde das vereinbarte Therapieziel erreicht, sodass die Versorgung mit einer Person (24-h-Hilfe) zu Hause wieder gesichert werden konnte. Auch die Beinödeme zeigten sich unter der Herzinsuffizienztherapie vollständig regredient, sodass sich die Beweglichkeit der Beine und die Belastbarkeit des Patienten (Ruhedyspnoe) verbesserten.
Beim Patienten 2 wurde durch das Training eine verbesserte, eigenständige Mobilität am Rollator ermöglicht. Stürze traten im Observierungszeitraum nicht mehr auf.
Diese Fallbeispiele zeigen, dass eine gezielte interdisziplinäre geriatrische Diagnostik und Therapie notwendig ist, um das komplexe Problem der Gangstörung mit drohender Immobilität zu bearbeiten mit dem Ziel, Alltagsfunktionen zu verbessern, Stürze zu vermeiden und letztendlich die Lebensqualität zu optimieren.
Literatur
- Isaacs B 1981, Is geriatris a sepciality? In: Arie A (Hrsg.) Health care oft he elderly. London: Croom Helm. S. 224-235)
- Fried LP, Tangen CM, Walston J, et al. Frailty in older adults: evidence for a phenotype. J Gerontol A Biol Sci Med Sci. 2001;56(3): M146-156.
- Santos-Eggimann B, Cuenoud P, Spagnoli J, Junod J. Prevalence of fraily in middle-aged and older community-dwelling Europeans living in 10 countries. J Gerontol A Biol Sci Med Sci. 2009;64(6): 675-681.
- Rosenberg IH. Sacropenia: origins and clinical relevance. J Nutr. 1997;127(5Suppl): 009S-991S.
- Volpato S, Bianchi L, Cherubini A, et al. Prevalence and clinical correlates of sarcopenia in community-dwelling older people: application of the EWGSOP definition and diagnostic algorithm. J Gerontol A Biol Sci Med Sci. 2014;69(4): 438-446.
- Anders J (2009) Immobilitätssyndrom. In: von Renteln-Kruse W (Hrsg.) Medizin des Alterns und des alten Menschen. Heidelberg: Steinkopf. S. 88-89.
- Rockwood K, Song X, MacKnight C, et al. A global clinical measure of fitness and frailty in elderly people. CMAJ. 2005;173(5): 489-495.
- Basic D, Shanley C. Frailty in an older inpatient population: using the clinical frailty scale to predict patient outcomes. J Aging Health. 2015; 27(4): 670-685.
- Bauer J, Biolo G, Cederholm T, et al. Evidence-based recommendations for optimal dietary protein intake in older people: a position paper from the PROT-AGE Study Group. J Am Med Dir Assoc. 2013;14(8): 542-559.

